
23.07.2020 by Dr. Gabriele Kaiser
Purity Determination 医薬品の重要性
ここ数ヶ月の製品回収の増加により、医薬品成分の純度がいかに重要であるかが改めて認識されている。示差走査熱量測定(DSC)は、標準物質を必要とせず、1回の測定で化合物の絶対純度を迅速に分析することができます。
ここ数ヶ月の製品回収の増加により、医薬品成分の純度がいかに重要であるかが改めて認識されている。不要な化学物質の存在は、たとえsmall の量であっても、医薬品の有効性と安全性に影響を及ぼす可能性がある。純度チェックには様々な分析技術が用いられる。その中でも示差走査熱量測定(DSC)は、標準物質を必要とせず、1回の測定で化合物の絶対純度を迅速に分析することができる。
不純物とは何か、どこから来るのか
ICHガイドライン(ICH=International Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use)によると、不純物とは「製品中の活性物質または賦形剤として定義された化学的実体でない...あらゆる成分」である。不純物は以下のように分類される:
- 有機不純物
- 無機不純物
- 残留溶媒
有機不純物は、出発物質、合成中間体、副生成物、分解生成物に由来する場合がある。無機不純物は製造工程から発生する可能性があり、触媒、ろ過助剤、無機塩、試薬などが含まれる。残留溶媒は、その名の通り、無機または有機の液体に含まれる残留物である。このリストのうち、無機不純物と残留溶剤の数は通常限られている。そして、それらは通常既知であり、容易に特定することができる。しかし、有機不純物の場合は事情が異なる。その数はほとんど無限であり、その性質は合成の反応条件や原料の性質などに強く依存する(1)。
Purity Determination USP <891> およびPh. Eur. 2.2.34
米国薬局方の<891>章や欧州薬局方の2.2.34章では熱分析が扱われている。主成分とともに融解する不純物(共晶不純物とも呼ばれる)の総量は、対応する融解ピークのプロファイルを分析することによって調べることができる。この計算は、不純物含有量の増加は融解効果の幅を広げるという事実に基づいています。さらに、ピークは低温側にシフトする(共晶系の融点降下のVan´t Hoff則、図1参照)。
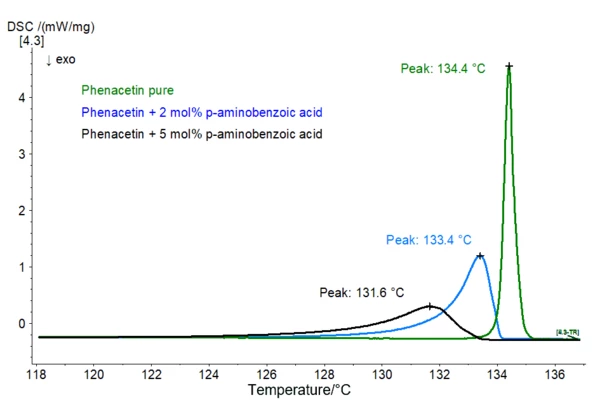
図1:純粋なフェナセチン(緑)、フェナセチン+2 mol% p-アミノ安息香酸(青)、フェナセチン+5 mol% p-アミノ安息香酸の融解効果の比較;試料質量:試料質量:1~1.3 mg、加熱速度:1 K/分:試料質量:1~1.3 mg、加熱速度:1 K/分、Al容器、N2雰囲気 Van´t Hoff方程式と純度の決定方法については、こちらを参照。この方法を適用する前提条件は、固溶体が形成されないこと、すなわち不純物が液相にのみ溶解し、固相には溶解しないことである。さらに、信頼できる結果を得るためには、以下の点を考慮する必要がある:
- 物質の純度は98.5%(USP <891>)または98%(Ph.Eur.2.2.34)以上であること。
- 物質は結晶質でなければならない(非晶質または部分的に非晶質であってはならない)。
- 材料は融解中に分解しないこと
- 多形性で存在する化合物は、完全に一つの形に変換されるべきである。
- 合成に由来する不純物は、主成分と同じような形や大きさを持ち、格子を破壊することなくそのマトリックスに適合することができる。このような不純物はDSCでは検出できない。
前述の薬局方の記述の他に、ASTM規格(ASTM E928)があり、融点が明確で熱的に安定な化合物の純度をDSCで測定する方法が詳細に記述されています。Purity Determination 、次回のブログで紹介する!文献:(1) ICH Topic Q 3 A (R2), 新薬中の不純物, EMEA, 2006年10月